Anomalies neurologiques et physiques mineures chez des patients présentant un premier épisode psychotique
Minor neurological and physical anomalies in patients with first-episode psychosis
| A. Mhalla, N. Boussaïd, L. Gassab, L. Gaha, A. Mechri Service de psychiatrie, CHU de Monastir, rue 1er-Juin, 5000 Monastir, Tunisie |
Télécharger l'article au format PDF
|
Résumé
Les objectifs de notre étude étaient de déterminer la prévalence, les scores, et la nature des signes neurologiques mineurs (SNM) et des anomalies physiques mineures (APM) chez des patients présentant un premier épisode psychotique et de rechercher les corrélations entre ces marqueurs et les caractéristiques des patients. Il s’agit d’une étude transversale portant sur 61 patients hospitalisés pour premier épisode psychotique. La procédure d’évaluation a consisté en la passation des échelles cliniques du fonctionnement prémorbide (PAS), des symptômes positifs et négatifs (PANSS), des impressions cliniques globales (CGI) et d’évaluation globale du fonctionnement (EGF) et des échelles des SNM de Krebs et al. et des APM de Gourion et al. La prévalence des SNM était de 83,6% avec un score total moyen de 15,3 ± 6,7. La prévalence des APM était de 62,7% avec un score total moyen de 5,8 ± 3,2. Des corrélations ont été trouvées entre les SNM et le mauvais fonctionnement prémorbide à la PAS, les dimensions négatives et de désorganisation à la PANSS, la gravité de la maladie à la CGI, l’altération du fonctionnement à l’EGF et les symptômes extrapyramidaux. Ces résultats rejoignent les données de la littérature rapportant des scores élevés des SNM et des APM chez les patients avec premier épisode psychotique. Les SNM, en particulier, semblent caractériser un processus physiopathologique plus sévère des troubles psychotiques et pourraient constituer un indicateur pronostique.
© L’Encéphale, Paris, 2012.
Summary
Introduction. — Over the last several decades, there has been an increasing number of neuroanatomical, neuroimaging, neurophysiological, and neuropsychological studies in search of structural, functional, and cognitive correlates of brain insult(s) that could ultimately lead to unravelling the pathophysiology of schizophrenia. A direct, easily administered, and inexpensive way of investigating brain dysfunction in schizophrenia is the study of neurological soft signs and minor physical anomalies, two putative indices of developmental abnormality. The study of these neurodevelopmental markers in the first-episode psychosis allows the detection of the neurodevelopmental abnormalities at the onset of psychosis.
Aims of the study. — The objectives of our study were to determinate the prevalence, the scores, and the nature of neurological soft signs (NSS) and minor physical anomalies (MPA) in patients with first-episode psychosis and to explore the correlations between these neurodevelopmental markers and the demographic, clinical and therapeutic features.
Method. — A cross-sectional study was carried-out on 61 patients (mean age: 28.9 ± 9.4 years; 86.9% were males), hospitalized for first-episode psychosis (DSM-IV-TR diagnosis of schizophrenia, schizophreniform disorder, brief psychotic disorder, delusional disorder, and psychotic disorder not otherwise specified). The evaluation procedure consisted of a retrospective assessment of the premorbid functioning by the Premorbid Functioning Scale (PAS) and the following clinical scales: Positive and Negative Symptoms Scale (PANSS), Clinical Global Impression (CGI) and Global Assessment of Functioning (GAF), the NSS scale of Krebs et al. (23 items exploring motor coordination, motor integrative function, sensory integration, involuntary movements or posture, quality of lateralization) and the MPA scale of Gourion et al. (41 items, exploring anomalies of face, eyes, ears, mouth, hands and feet).
Results. — The prevalence of NSS was 83.6% (cut-off point = 9.5), with a mean total score of 15.3 ± 6.7. The highest score was for the motor coordination. The prevalence of MPA was 62.7% (cut-off point = 5), with a mean total score of 5.8 ± 3.2. The most common MPA were the fine hair (50.8%), adherent earlobes (49.2%) and clinodactyly (31.1%). Correlations were found between the NSS total score and the Poor Premorbid Functioning (r = 0.32, P = 0.04), the PANSS total score (r = 0.36, P = 0.005), and the negative (r = 0.45, P < 0.001) and disorganization sub-scores (r = 0.41, P = 0.001), the CGI-severity of (r = 0.30, P = 0.02), the impairment functioning in the GAF (r = −0.26, P = 0.04) and with extrapyramidal symptoms (r = 0.52, P < 0.001). However, no correlation was found between the NSS total scores, age, gender, the PANSS positive sub-score, the daily dosage of antipsychotics, the CGI-improvement score and the MPA total score. There was no correlation between MPA total score and demographic, clinical and therapeutic features of patients. Moreover, there was no correlation between the NSS or MPA scores and the short-term evolution (6 months to 1 year) towards schizophrenia.
Conclusion. — These results confirm the data in the literature relating high NSS and MPA scores in patients with a first-episode psychosis. The NSS appear to characterize severe psychotic disorders with more negative and disorganization symptoms and poor social functioning and may be a prognostic indicator.
© L’Encéphale, Paris, 2012.
Introduction
Un intérêt croissant concerne le dépistage des signes précoces marquant le début de la schizophrénie et l’étude des modes d’entrée dans la maladie. Cet intérêt pour les phases précoces de la maladie dénote de la complexité physiopathologique et de l’hétérogénéité phénotypique de la schizophrénie.
Plusieurs études ont mis en évidence des anomalies du neurodéveloppement cérébral chez les patients atteints de schizophrénie qui se traduisent par des marqueurs cliniques, cognitifs, électrophysiologiques et neuroanatomiques [1—4]. Parmi ces marqueurs dits « neurodéveloppementaux », les signes neurologiques et les anomalies physiques mineurs sont d’évaluation facile et peu coûteuse. Les signes neurologiques mineurs (SNM) ou soft signs, par opposition aux signes « majeurs », correspondent à des anomalies qui ne peuvent pas être directement reliées au dysfonctionnement d’une région précise du cerveau ou qui n’appartiennent pas à un syndrome neurologique particulier [5—7]. Cette définition « non localisatrice » reflète la difficulté à déterminer les circuits mis en jeu dans ces anomalies. Quant aux anomalies physiques mineures (APM), ce sont des dysmorphies discrètes, présentes dans différentes régions du corps (face, mains, pieds), qui reflètent une altération subtile du développement des tissus mous et des structures cartilagineuses et osseuses. Ce sont des erreurs de la morphogenèse qui surviennent au cours du premier trimestre et au début du second trimestre de la gestation ; leur présence suggère une altération précoce du développement du neuroectoderme [8—10]. L’étude de ces marqueurs neurodéveloppementaux dans le premier épisode psychotique permettrait de vérifier leur existence chez les patients présentant un risque accru de développer la schizophrénie.
Les objectifs de notre étude étaient de déterminer la prévalence, les scores, et la nature des SNM et des APM chez un groupe de patients présentant un premier épisode psychotique et de rechercher les corrélations entre ces marqueurs et les caractéristiques sociodémographiques, cliniques, thérapeutiques et évolutives des patients.
Patients et méthode
Il s’agit d’une étude transversale, descriptive et analytique, réalisée au service de psychiatrie du CHU de Monastir, durant la période allant de juillet 2009 à septembre 2010 portant sur les patients hospitalisés pour un premier épisode psychotique (n = 61). Ces patients ont répondu aux critères DSM-IV-TR [11] de l’un des troubles suivants : trouble psychotique bref (n = 10), trouble schizophréniforme (n = 26), schizophrénie (n = 20), trouble délirant (n = 1) ou trouble psychotique non spécifié (n = 4). Il s’agit du diagnostic retenu à la sortie des patients par consensus de l’équipe médicale du service. Les patients non consentants ou non coopérants, les patients ayant un retard mental ou des anomalies cérébrales d’origine métabolique, neurologique ou traumatique et les patients ayant un épisode thymique avec caractéristiques psychotiques ou une schizophrénie évoluant depuis plus de deux ans ont été exclus.
Les données épidémiologiques et cliniques ont été recueillies à l’aide d’une fiche préétablie remplie à partir de l’interrogatoire du patient, des membres de sa famille et de la revue du dossier médical. Nous avons aussi procédé à une évaluation rétrospective du fonctionnement prémorbide à l’aide de l’échelle Premorbid Adjustment Scale (PAS) de Foerster et al. [12] et une évaluation psychométrique par les échelles : Positive and Negative Symptoms Scale (PANSS) [13] et Évaluation Globale du Fonctionnement (EGF) [11]. La passation de ces échelles a été effectuée, par le même évaluateur, dans les trois jours succédant à l’hospitalisation.
L’évaluation des SNM a été réalisée par l’échelle de Krebs et al. [5] comportant 23 SNM cotés de 0 à 3 et explorant cinq dimensions : coordination motrice, intégration motrice, intégration sensorielle, mouvements involontaires et qualité de latéralisation et dix signes extrapyramidaux, utilisant les items de l’échelle Simpson et Angus.
L’évaluation des APM a été effectuée par l’échelle de Gourion et al. [8] comportant 41 items permettant de rechercher des APM dans les six régions du corps : face, yeux, oreilles, bouche, mains et pieds. Les évaluations des SNM et des APM ont été accomplies, par le même évaluateur, dans les sept jours succédant à l’hospitalisation.
L’évolution sous traitement a été appréciée à la sortie des patients par le remplissage des Impressions Cliniques Globales (CGI) [14] et à moyen terme à partir des observations du médecin traitant lors des consultations de postcure, en précisant la durée du suivi après l’hospitalisation (en mois).
L’analyse des données a été effectuée à l’aide du logiciel SPSS 10.0. (Norusis/SPSS Inc., 1992) avec une analyse descriptive des différentes variables et une analyse analytique en utilisant le test Chi2 , le test « t » de Student et le coefficient de corrélation « r » de Pearson. En cas de distribution non gaussienne des variables, des tests non paramétriques ont été utilisés. Nous avons fixé un seuil de 5% pour les associations significatives.
Résultats
Description de la population d’étude
Notre population était majoritairement masculine (86,9%), avec un âge moyen de 28,9 ± 9,4 ans (des extrêmes de 18 et
54 ans). La plupart des patients étaient célibataires (75,4%) et sans emploi (55,8%). Les scores totaux moyens de la PAS augmentaient avec l’âge : de 16,4 entre cinq et 11 ans à 21,2 entre 16 et 20 ans, indiquant une altération progressive du fonctionnement à l’approche des troubles. Le score total moyen de la PANSS était de 99,5 ± 20,6, avec une prédominance de la symptomatologie positive chez 64,1% des patients. Le score moyen à l’EGF était de 33 ± 8 avec des extrêmes de 20 et 50. La plupart des patients (77%) étaient manifestement ou gravement malades à la CGI-gravité.
Tous les patients ont été hospitalisés, avec une durée moyenne de séjour de 29,1 ± 16,6 jours (des extrêmes de cinq et 64 jours). Sur le plan thérapeutique, 31,1% des patients ont bénéficié d’un traitement antipsychotique atypique en monothérapie, 29,5% d’un traitement neuroleptique classique en monothérapie et les autres patients étaient sous association d’antipsychotiques. La posologie moyenne était de 619,8 ± 419,8 mg en équivalent chlorpromazine. Ce traitement antipsychotique a été instauré au moment de l’hospitalisation pour la majorité des patients (67,2%). Pour 24,6% des patients, un traitement antipsychotique a été administré dans les jours ou les semaines précédant l’hospitalisation, alors que les autres patients avaient reçu un traitement antidépresseur ou anxiolytique avant l’hospitalisation.
Sous traitement, 72,1% des patients étaient fortement à très fortement améliorés à la CGI-amélioration. Le score moyen à l’échelle de Simpson et Angus était de 3,8 ± 3,3. Sur le plan évolutif, le suivi à moyen terme, entre six mois et un an (avec une médiane à huit mois), a objectivé une évolution vers la schizophrénie chez 35% des patients qui avaient initialement un autre diagnostic (n = 40). Les autres patients étaient en rémission (40%), en rechute (12,5%) ou perdus de vue (10%).
Prévalence et scores des marqueurs neurodéveloppementaux
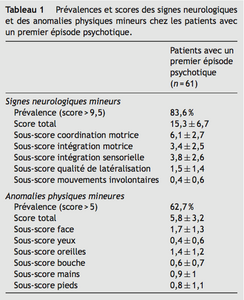
La prévalence des SNM était de 83,6%, en adoptant le score seuil de 9,5. Le score total moyen était de 15,3 ± 6,7, avec des extrêmes de 4 et 32,5. En fonction des dimensions des SNM, le sous-score le plus élevé concernait les anomalies de la coordination motrice avec un score moyen de 6,1 ± 2,7 (Tableau 1). La prévalence des APM était de 62,7% en considérant le score seuil de 5. Le score total moyen des APM était de 5,8 ± 3,2 avec des extrêmes de 1 et 14. En fonction de la topographie, les sous-scores les plus élevés concernaient les anomalies de la face (1,7 ± 1,3). Les APM les plus fréquentes étaient les cheveux fins (50,8%), les lobules adhérents (49,2%) et la clinodactylie (31,1%) (Tableau 1).
Corrélations entre marqueurs neurodéveloppementaux et caractéristiques des patients
Le score total des SNM était corrélé au bas niveau scolaire (p = 0,02) et au mauvais fonctionnement prémorbide (selon les scores de la PAS) (p = 0,04). Les sous-scores « intégration motrice » et « intégration sensorielle » étaient aussi corrélés au mauvais fonctionnement prémorbide surtout entre 12 et 15 ans (respectivement p = 0,04 et p = 0,004).
Une relation complexe a été établie avec les conduites addictives. Ainsi, le score total des SNM était significativement plus élevé chez les patients consommateurs d’alcool (16,7 ± 6,7 versus 12,9 ± 5,6, p = 0,02) ; il était significativement moins élevé chez les patients consommateurs de cannabis (11,2 ± 5,6 versus 16 ± 6,7, p = 0,04).
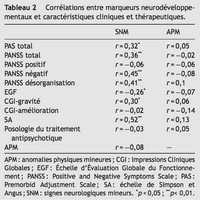
Selon les caractéristiques cliniques, le score total des SNM était corrélé au score total (p = 0,005) et aux dimensions négative (p < 0,001) et de désorganisation (p = 0,001) de la PANSS, à la sévérité de la maladie (selon le score de la CGI-gravité) (p = 0,02) et à l’altération du fonctionnement (selon le score de l’EGF à l’admission) (p = 0,04) (Tableau 2).
Selon les caractéristiques thérapeutiques, les scores des symptômes extrapyramidaux à l’échelle Simpson et Angus étaient corrélés au score total des SNM (p < 0,001) ainsi qu’aux sous-scores des dimensions « coordination motrice » (p = 0,003), « intégration motrice » (p < 0,001) et « intégration sensorielle » (p = 0,001). En revanche, nous n’avons pas trouvé de corrélation entre les scores des SNM et les autres caractéristiques thérapeutiques (type et posologie du traitement antipsychotique), la réponse au traitement (selon le score de la CGI-amélioration) et l’évolution vers une schizophrénie à moyen terme.
Quant aux APM, aucune corrélation n’a été trouvée avec les caractéristiques anamnestiques, cliniques, thérapeutiques et évolutives des patients. De même, il n’y avait pas de corrélation entre le score total des APM et le score total des SNM (Tableau 2).
Discussion
Dans ce travail, des scores élevés des SNM et des APM ont été trouvés chez des patients hospitalisés pour un premier épisode psychotique. Des associations ont été établies entre les SNM et le mauvais fonctionnement prémorbide, la présence de symptômes négatifs et de désorganisation, la gravité de la maladie, le mauvais fonctionnement social et la présence d’effets extrapyramidaux. Alors que, les APM n’étaient pas associés aux caractéristiques cliniques et thérapeutiques des patients.
Des limites méthodologiques devraient être prises en considération dans l’interprétation des résultats de notre travail : la taille relativement réduite de notre population d’étude, le recrutement exclusivement hospitalier, l’absence de groupe témoin de comparaison, l’évaluation rétrospective des caractéristiques anamnestiques, la non-utilisation des questionnaires diagnostiques standardisés et l’absence de suivi longitudinal à long terme.
Dans notre étude, la prévalence des SNM était de 83,6%, compte tenu du score seuil de 9,5 préconisé par l’auteur [5]. Dans la littérature, les études qui ont évalué les patients avec un premier épisode psychotique ont rapporté des prévalences élevées des SNM variant de 20% à 97,1% [15,16]. Pour les scores, plusieurs études [4,17—19] utilisant diverses échelles ont trouvé des scores élevés des SNM dans le premier épisode psychotique.
Dans notre étude, la prévalence des APM était de 62,7% en utilisant l’échelle de Gourion et al., avec le score seuil de 5 préconisé par les auteurs [8]. Lloyd et al. [20] ont rapporté une fréquence plus élevée des APM chez des patients présentant un premier épisode psychotique par rapport à des témoins sains. Dans une étude de cohorte [21], un taux plus important des APM était constaté chez les enfants ayant développé ultérieurement des troubles du spectre schizophrénique. En ce qui concerne les scores, à notre connaissance, il n’y a pas de travaux qui ont utilisé la même échelle des APM lors du premier épisode psychotique. Cependant, des études utilisant d’autres échelles ont trouvé des scores plus élevés des APM chez les patients avec premier épisode psychotique par rapport à des témoins sains [3,22,23].
Dans notre étude, nous n’avons pas trouvé de corrélation entre le score total des SNM et le score total des APM. Dans la littérature, cette relation n’a pas été explorée chez les patients avec premier épisode psychotique. En revanche, chez les patients schizophrènes, certains travaux ont constaté l’existence d’une corrélation entre ces deux marqueurs [3,24], alors que d’autres études n’ont pas trouvé cette relation, suggérant qu’il s’agit des marqueurs distincts ou indépendants [10,25].
Concernant la relation avec les caractéristiques de nos patients, les SNM étaient associés au mauvais fonctionnement prémorbide, ce qui rejoint les résultats d’autres auteurs [26]. Cependant, comme McGrath et al. [27], nous n’avons pas trouvé d’association entre fonctionnement prémorbide et APM. Pour la relation avec la consommation de toxiques, nos résultats rejoignent ceux de Ruiz-Veguilla et al. [28] rapportant un score moins élevé des SNM chez les patients consommateurs de cannabis.
Dans notre étude, le score total des SNM était corrélé au score total de la PANSS et aux scores des dimensions négatives et de désorganisation de la PANSS. Il n’y avait pas de corrélation avec le score de la dimension positive. Selon plusieurs revues de la littérature [6,15,29,30], la plupart des études n’ont pas relevé de corrélation entre les scores des SNM et la dimension positive dans le premier épisode psychotique. Cette absence de corrélation serait expliquée par la fluctuation importante des symptômes positifs au cours de l’évolution d’un processus psychotique, alors que les SNM sont considérés des marqueurs-traits stables. Par ailleurs, la plupart des auteurs ont établi une corrélation entre les scores des SNM et les symptômes négatifs et de désorganisation dans la schizophrénie et dans le premier épisode psychotique [6,7,15,29,31,32].
Le score total des SNM était aussi corrélé au score de la CGI-gravité et au score de l’EGF à l’admission dans notre étude. Dans la revue de littérature de Dazzan et Murray [15], la plupart des études ont conclu à une corrélation entre les SNM et la gravité du premier épisode psychotique. Ces données soulignent l’intérêt pronostique des SNM, confirmé par des études récentes mettant en évidence des corrélations entre SNM et anomalies cérébrales chez les patients avec premier épisode psychotique [33,34].
Pour les APM, il n’y avait pas de corrélation avec les scores de la PANSS, de la CGI-gravité et de l’EGF dans notre travail. D’autres études ont aussi conclu à l’absence de corrélation entre les scores des APM et les différents scores de la PANSS [27,35]. En revanche, certains auteurs ont rapporté une association entre les APM et les symptômes négatifs [9,36]. Quant à l’absence de corrélation avec le score de la CGI-gravité, Kébir et al. [37] ont rapporté le même résultat chez des patients schizophrènes.
Nous n’avons pas trouvé de corrélation entre les scores des SNM et la posologie journalière du traitement antipsychotique, ce qui est en accord avec les données de la littérature [6,29]. Le score des symptômes extrapyramidaux à l’échelle Simpson et Angus était corrélé au score total des SNM dans notre étude. D’après la revue de la littérature de Bombin et al. [29], cinq études ont trouvé cette association contre cinq études négatives. Toutefois, la présence des signes extrapyramidaux serait plus liée au trouble psychotique qu’au traitement antipsychotique. En effet, Peralta et al. [26,38] ont récemment établi une association entre signes parkinsoniens et SNM chez des patients psychotiques jamais traités. Pour la réponse au traitement, il n’y avait pas de corrélation entre le score CGI-amélioration et les différents scores des SNM dans notre étude, alors que Prikryl et al. [39] ont trouvé des scores plus élevés des SNM chez les patients ayant une évolution chronique par rapport à ceux en rémission de leur premier épisode psychotique.
Pour les APM, il n’y avait pas de corrélation avec la posologie journalière des antipsychotiques, le score à l’échelle Simpson et Angus, et le score CGI-amélioration. Dans la littérature, peu d’études se sont intéressées à la relation entre les APM et les caractéristiques thérapeutiques. Lohr et Flynn [35] ont rapporté que les patients schizophrènes avec dyskinésie tardive avaient plus d’APM que les autres patients. Pour leur part, McGrath et al. [27] ont montré que les patients schizophrènes avec un score élevé des APM avaient une mauvaise réponse au traitement antipsychotique.
L’absence de différence, dans notre étude, au niveau des scores des SNM et des APM entre les patients diagnostiqués avec schizophrénie et ceux ayant une rémission de leurs troubles pourrait s’expliquer par la taille réduite des sous-groupes et l’absence de suivi au long cours. Ainsi, un suivi longitudinal est nécessaire pour évaluer l’intérêt de ces marqueurs comme facteurs prédictifs de l’évolution d’un premier épisode psychotique.
Conclusion
Les prévalences et les scores élevés des SNM et des APM dans le premier épisode psychotique renforcent la place de ces marqueurs comme indicateurs de vulnérabilité à la schizophrénie. Nos résultats suggèrent que les SNM pourraient caractériser un processus physiopathologique plus sévère des troubles psychotiques débutants avec des symptômes négatifs et de désorganisation plus marqués et un mauvais fonctionnement social ; ainsi, ils pourraient constituer un indicateur pronostique péjoratif. Les signes neurologiques et les anomalies physiques mineurs semblent être des marqueurs indépendants, mais qui pourraient offrir une meilleure valeur prédictive s’ils étaient considérés comme un phénotype composite.
Références
[1] Gourion D, Gourevitch R, Leprovost JB, et al. L’hypothèse neurodéveloppementale dans la schizophrénie. Encéphale 2004;30(2):109—18.
[2] Thibaut F. Hypothèse neurodéveloppementale de la schizophrénie. Encéphale 2006;32:879—82.
[3] John JP, Arunachalam V, Ratnam B, et al. Expanding the schizophrenia phenotype: a composite evaluation of neurodevelopmental markers. Compr Psychiatry 2008;49:78—86.
[4] Keshavan M, Sanders R, Sweeney JA. Diagnostic specificity and neuroanatomical validity of neurological abnormalities in first-episode psychoses. Am J Psychiatry 2003;160:1298—304.
[5] Krebs MO, Gut-Fayand A, Bourdel MC, et al. Validation and factorial structure of a standardized neuroligical examination assessing neurological soft signs in schizophrenia. Schizophr Res 2000;45:245—60.
[6] Krebs MO, Mouchet S. Signes neurologiques mineurs et schizophrénie : revue des données actuelles. Rev Neurol 2007;163:1157—68.
[7] Mechri A, Slama H, Bourdel MC, et al. Signes neurologiques mineurs chez les patients schizophrènes et leurs apparentés non malades. Encéphale 2008;34:483—9.
[8] Gourion D, Viot G, Goldberger C, et al. Validation française d’une échelle d’anomalies physiques mineures appliquée à des patients schizophrènes et à leurs parents. Encéphale 2001;27(2):134—7.
[9] O’Callaghan E, Larkin C, Kinsella A, et al. Familial, obstetric, and other clinical correlates of minor physical anomalies in schizophrenia. Am J Psychiatry 1991;148:479—83.
[10] Compton MT, Chan RC, Walker EF, et al. Minor physical anomalies: potentially informative vestiges of fetal developmental disruptions in schizophrenia. Int J Dev Neurosci 2011;29(3):245—50.
[11] American Psychiatric Association. Manuel diagnostique et statistique des troubles mentaux : texte révisé. DSM-IV-TR 2e éd. Paris: Masson; 2003.
[12] Foerster A, Lewis S, Owen M, et al. Pre-morbid adjustment and personality in psychosis effects of sex and diagnosis. Br J Psychiatry 1991;158:171—6.
[13] Kay SR, Fizbein A, Opler LA. The positive and negative syndrome scale (PANSS) for schizophrenia. Schizophr Bull 1987;13:261—76.
[14] Guelfi JD. L’évaluation clinique standardisée en psychiatrie, II. Lavaur: Ed. Pierre Fabre; 1997, p. 585—91.
[15] Dazzan P, Murray R. Neurological soft signs in first-episode psychosis: systematic review. Br J Psychiatry 2002;181: 50—7.
[16] Browne S, Clarke M, Gervin M, et al. Determinants of neurological dysfunction in first-episode schizophrenia. Psychol Med 2000;30:1433—41.
[17] Bachmann S, Bottmer C, Schröder J. Neurological soft signs in first-episode schizophrenia: a follow-up study. Am J Psychiatry 2005;162:2337—43.
[18] Dazzan P, Lloyd T, Morgan KD. Neurological abnormalities and cognitive ability in first-episode psychosis. Br J Psychiatry 2008;193:197—202.
[19] Emsley R, Turner HJ, Oosthuizen PP, et al. Neurological abnormalities in first-episode schizophrenia: temporal stability and clinical and outcome correlates. Schizophr Res 2005;75: 35—44.
[20] Lloyd T, Dazzan P, Dean K, et al. Minor physical anomalies in patients with first-episode psychosis: their frequency and diagnostic specificity. Psychol Med 2008;38(1):71—7.
[21] Schiffman J, Ekstrom M, LaBrie J. Minor physical anomalies and schizophrenia spectrum disorders: a prospective investigation. Am J Psychiatry 2002;159:238—43.
[22] McGrath JJ, El-Saadi O, Grim V, et al. Minor physical anomalies and quantitative measures of the head and face in patients with psychosis. Arch Gen Psychiatry 2002;59(5): 458—64.
[23] Dean K, Dazzan P, Lloyd T, et al. Minor physical anomalies across ethnic groups in a first episode psychosis sample. Schizophr Res 2007;89:86—90.
[24] Gourion D, Goldberger CC, Olié JP, et al. Neurological and morphological anomalies and the genetic liability to schizophrenia: a composite phenotype. Schizophr Res 2004;67:23—31.
[25] Aksoy-Poyraz C, Poyraz BÇ, Turan Ş, et al. Minorphysical anomalies and neurological soft signs in patients with schizophrenia and their siblings. Psychiatry Res 2011;190(1):85—90.
[26] Peralta V, de Jalón EG, Campos MS, et al. Risk factors, premorbid functioning and episode correlates of neurological soft signs in drug-naive patients with schizophrenia-spectrum disorders. Psychol Med 2010;22:1—11.
[27] McGrath JJ, Van Os J, Hoyos C, et al. Minor physical anomalies in psychoses: associations with clinical and putative aetiological variables. Schizophr Res 1995;18:9—20.
[28] Ruiz-Veguilla M, Gurpegui M, Barrigón ML, et al. Fewer neurological soft signs among first episode psychosis patients with heavy cannabis use. Schizophr Res 2009;107:158—64.
[29] Bombin I, Arango C, Buchanan R. Significance and meaning of neurological signs in schizophrenia: two decades later. Schizophr Bull 2005;31:962—77.
[30] Tosato S, Dazzan P. The psychopathology of schizophrenia and the presence of neurological soft signs: a review. Curr Opin Psychiatry 2005;18:285—8.
[31] Krebs MO, Gut-Fayan A, Bourdel MC, et al. Desorganisation syndrom is correlated to sensory neurological soft signs in medicated and neuroleptic naive schizophrenic patients. Schizophr Res 2002;53:232.
[32] Ruiz-Veguilla M, Cervilla JA, Barrigon ML, et al. Neurodevelopmental markers in different psychopathological dimensions of first episode psychosis: the ESPIGAS study. Eur Psychiatry 2008;23:533—40.
[33] Kong L, Bachmann S, Thomann PA, et al. Neurological soft signs and gray matter changes: a longitudinal analysis in first-episode schizophrenia. Schizophr Res 2012;134:27—32.
[34] Mouchet-Mages S, Rodrigo S, Cachia A, et al. Correlations of cerebello-thalamo-prefrontal structure and neurological soft signs in patient with first-episode psychosis. Acta Psychiatr Scand 2011;123(6):451—8.
[35] Lohr JB, Flynn K. Minor physical anomalies in schizophrenia and mood disorder. Schizophr Bull 1993;19(3):550—6.
[36] Hata K, Iida J, Iwasaka H. Association between minor physical anomalies and lateral ventricular enlargement in childhood and adolescent onset schizophrenia. Acta Psychiatr Scand 2003;108(2):147—51.
[37] Kébir O, El-Hechmi Z, Kébir H, et al. Les anomalies morphologiques mineures dans la schizophrénie : étude d’une population tunisienne. Ann Med Psychol 2006;164:383—7.
[38] Peralta V, Basterra V, Campos MS, et al. Characterization of spontaneous Parkinsonism in drug-naive patients with nonaffective psychotic disorders. Eur Arch Psychiatry Clin Neurosci 2012;262(2):131—8.
[39] Prikryl R, Ceskova E, Tronerova S, et al. Dynamics of neurological soft signs and its relationship to clinical course in patients with first-episode schizophrenia. Psychiatry Res 2012 http://dx.doi.org/10.1016/j.psychres.2012.03.008.